业务咨询

![]() 发布时间:2025-09-15
发布时间:2025-09-15
![]() 环特生物
环特生物
![]() 浏览次数:20
浏览次数:20
原创:陈将飞等首席科研官

编者按
对苯二胺类化合物(PPDs)是一种在橡胶工业(尤其轮胎制造)中被广泛应用的抗氧化剂,作为公认的环境污染物,它对野生动物和人类健康造成了潜在的风险。目前,在车辆粉尘、地表径流、废水及灰尘等环境介质中已广泛检出N-环己基-N-苯基对苯二胺(CPPD)、N-异丙基-N'-苯基对苯二胺(IPPD)、N,N'-双(1,4-二甲基戊基)-对苯二胺(77PD)等多种PPDs,但现有大部分研究集中于N-1,3-二甲基丁基-N'-苯基对苯二胺(6PPD),而这几种PPDs的生态毒理学效应及其作用机制尚不清楚。
8月23日,环特生物长期合作伙伴——浙江省模式生物技术与应用重点实验室、温州医科大学的陈将飞副研究员团队联合中国科学院生态环境研究中心国家重点实验室,在前期连发3篇TOP一区环境毒理学论文的基础上,又在国际权威期刊《Journal of Hazardous Materials》(IF=12.2)上发表最新研究成果《Gut-brain axis dysfunction mediates neurotoxicity of embryonic p-phenylenediamine exposure in zebrafish》。该研究基于斑马鱼模型,系统探究了三种对苯二胺类抗氧化剂PPDs——CPPD、IPPD、77PD通过肠-脑轴功能紊乱导致斑马鱼神经毒性及其作用机制,首次揭示了PPDs通过破坏肠道菌群-脑轴而导致神经毒性,为评估PPDs类污染物的生态与健康风险提供了重要科学依据。
本研究中,通过斑马鱼模型进行了多维度毒性评估,发现斑马鱼胚胎暴露于PPDs会破坏肠-脑轴功能,导致持久性的斑马鱼生长抑制和行为异常,揭示了肠-脑轴功能紊乱是PPDs介导神经毒性的关键机制。(环境中风险物质的斑马鱼胚胎急性毒性评价及甲状腺干扰效应评估)
01、研究亮点
• 首次系统评估了CPPD、IPPD、77PD这三种较少被关注的PPDs的斑马鱼神经毒性,并进行了多维度毒性评估,证实了PPDs会引起生长抑制和行为异常、脑部氧化应激和神经细胞损伤、肠道结构损伤和菌群失调等;
• 首次利用斑马鱼模型揭示了PPDs通过破坏肠道菌群-脑轴导致神经行为异常,并利用qPCR和ELISA实验,以及抗生素甲硝唑(MTZ)干预实验验证了该机制;
• 通过双组学整合分析等,强有力地支持了肠-脑轴在PPDs神经毒性中的核心作用 ,为理解环境污染物的毒性机制提供了新视角。
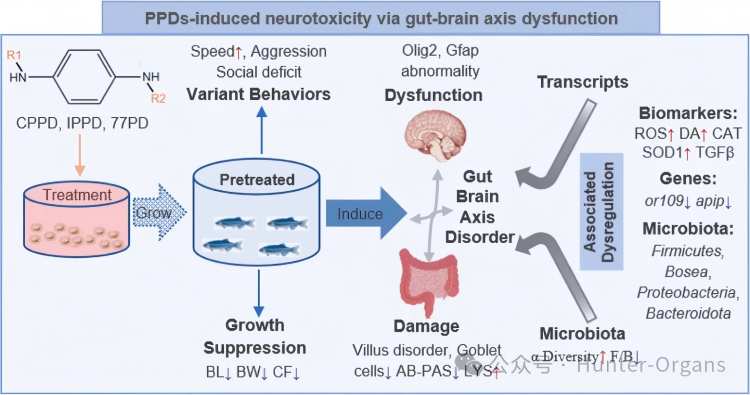
图形摘要
02、主要研究成果
1. PPDs暴露引起斑马鱼生长抑制与行为异常
研究人员将胚胎期的斑马鱼暴露于CPPD、IPPD和77PD后发现,这显著影响了斑马鱼的生长和行为反应。具体而言,在生长抑制方面,CPPD暴露显著降低了斑马鱼的体重、体长和条件因子(CF),表明斑马鱼的发育受损最严重,而IPPD和77PD也受到不同程度的影响。
行为方面,CPPD和IPPD处理组的游泳模式发生了显著变化,平均游泳速度均有所提高,且对光照更敏感,而77PD无显著影响;CPPD增加镜面攻击行为,而77PD则与之相反,攻击性降低;所有PPDs均负向影响了社会接触行为,CPPD和77PD暴露显著减少了社交接触频率和持续时间;在趋近行为测试中,IPPD和77PD处理组破坏了正常的社交模式,表现为增加最近邻距离(NND)和个体间距离(D),这表明社交凝聚力下降。这些发现表明,不同的PPDs会引发独特的行为异常模式。

图1
2. PPDs暴露诱导眼-脑轴神经细胞异常
Olig2是少突胶质细胞分化过程中起关键作用的转录因子,在髓鞘形成中起重要作用,Gfap作为胶质纤维酸性蛋白,则是星形胶质细胞的标志物。Gfap或Olig2异常通常发生在神经炎症、脑水肿引起的疾病和创伤性脑损伤中。本研究中,研究人员通过使用双标记转基因斑马鱼,分别对暴露于CPPD、IPPD和77PD的斑马鱼胚胎进行研究,发现在PPDs处理组中,Gfap和Olig2的眼-脑轴表达模式发生了显著变化。
具体而言,定量分析显示,CPPD组的头部重量显著降低;所有PPDs组中,少突胶质细胞标志物Olig2表达升高,IPPD还引起星形胶质细胞标志物Gfap表达异常。在视神经区域,Olig2表达受PPDs显著影响,CPPD中表达系乱,IPPD和77PD中的表达水平低,且出现断裂。这表明,PPDs可能干扰神经发育,特别是髓鞘形成和神经胶质细胞功能。
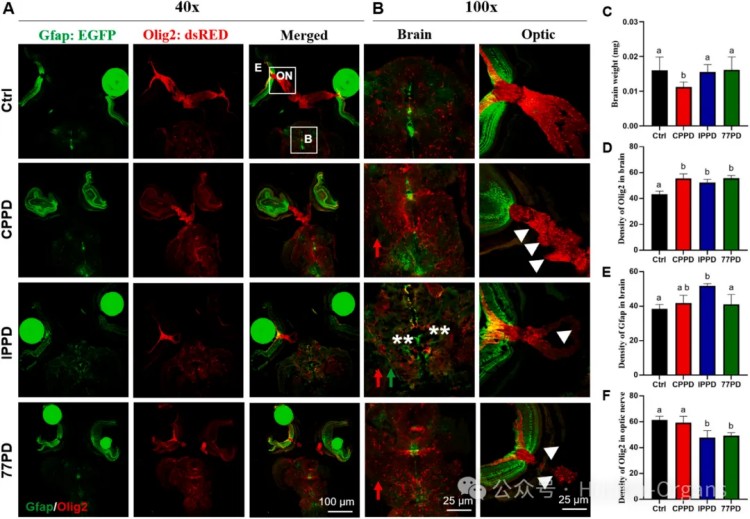
图2
3. PPDs暴露引起肠道损伤和功能障碍
暴露于PPDs会影响斑马鱼肠道的发育。具体而言,PPDs显著抑制了斑马鱼肠道的长度(P<0.05)。通过组织病理学分析发现,PPDs暴露导致绒毛结构扭曲,间隙增大,从而导致鱼肠道受损,影响了肠道功能。尤其在CPPD和IPPD处理组中,绒毛的高度显著增加,而在77PD处理组中则显著降低(P<0.05)。绒毛的宽度在PPDs中有所增加,其中CPPD和IPPD处理组的差异显著(P<0.05)。三个PPDs处理组的杯状细胞数量均显著减少(P<0.05),黏液分泌也均显著减少,进一步提示肠道屏障功能受损(P<0.05)。这表明,PPDs不仅损伤肠道结构,还破坏其黏液保护层等关键功能。

图3
4. PPDs暴露改变头部转录组,并改变肠道微生物群落
接着,研究人员利用头部和肠道微生物组的转录组数据,探究了PPDs的潜在机制。三种PPDs共同差异基因仅25个,两两之间重叠比例也较低。其中,CPPD和IPPD影响视觉通路;CPPD和77PD影响嗅觉与GPCR信号通路。这表明,不同的PPDs诱导了特定的、部分重叠的分子反应,这提示它们的作用机制存在差异。
肠道微生物组分析显示,PPDs诱发肠道菌群失调。三种PPDs的α多样性均有所增加,细菌种类组成发生变化。值得注意的是,在所有PPDs处理下,微生物群落中肠道菌群α多样性增加,β多样性显著改变。在所有PPDs处理中,有益菌,如Fusobacteriota、Cetobacterium均显著减少;有害菌Proteobacteria、潜在致病菌(Proteobacteria、Bacteroidota)均有所增加。PPDs处理鱼类肠道中Firmicutes/Bacteroidetes(F/B)比率降低,可能与生长抑制相关。这表明,PPDs诱导了肠道菌群失调,改变了有益菌和潜在致病菌的比例,这可能与生长抑制和肠道功能障碍有关。
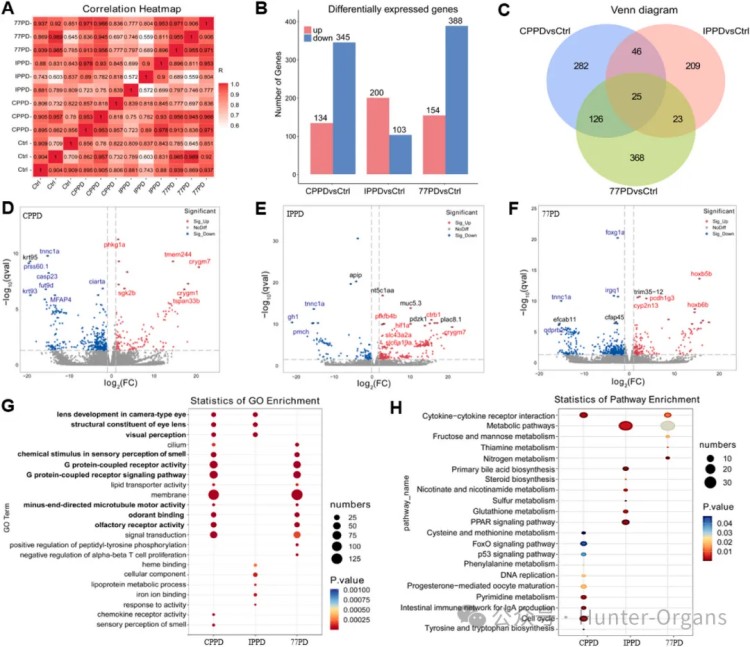
图4

图5
5. PPDs通过肠-脑轴功能障碍引起斑马鱼神经毒性
为了探究PPDs诱导神经毒性的分子机制,特别是肠道菌群与大脑基因表达的关联,研究人员整合头部分子组学数据和肠道微生物组数据进行相关性分析,发现了特定属级细菌与头部分子标志物之间的显著调控关系。例如,Bacteroidota属与多个头部分子标志物,如ROS、DA、TGFB、SOD1、CAT存在显著关联;Firmicutes属与ROS等肠道损伤标志物关联密切。这些关联的蛋白互作网络,揭示了潜在的调控通路。这证实了PPDs通过影响肠道菌群,进而影响大脑基因表达和功能,支持了肠-脑轴在PPDs神经毒性中的作用。
随后,研究人员利用实时定量PCR法(qPCR)与酶联免疫吸附试验 (ELISA)进行了验证,针对肠道和头部的qPCR和ELISA检测结果显示,CPPD具有最多的显著标志物,其次是77PD,然后是IPPD,这表明在所有PPDs中,CPPD在肠道中引发的炎症反应最为明显,77PD对肠道的影响要大于对头部的影响。肠道生物标志物之间相关性最高,其次是肠道与头部生物标志物。因此,多种验证手段相互印证,进一步支持了PPDs通过引起肠道炎症、氧化应激、神经递质失衡等途径,影响大脑功能。
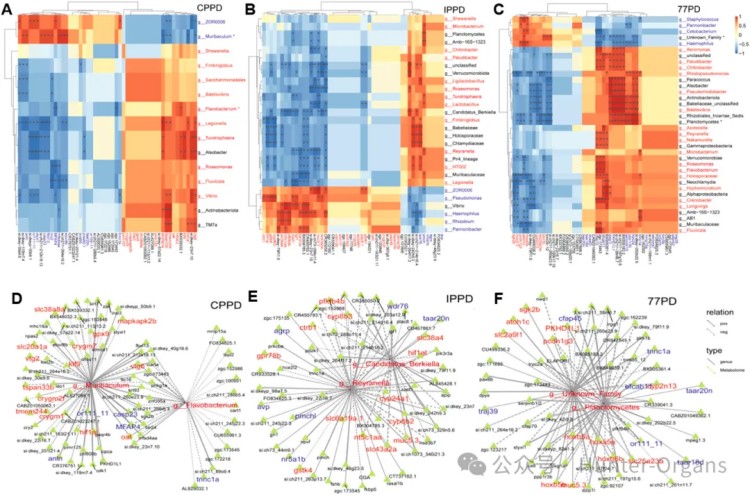
图6
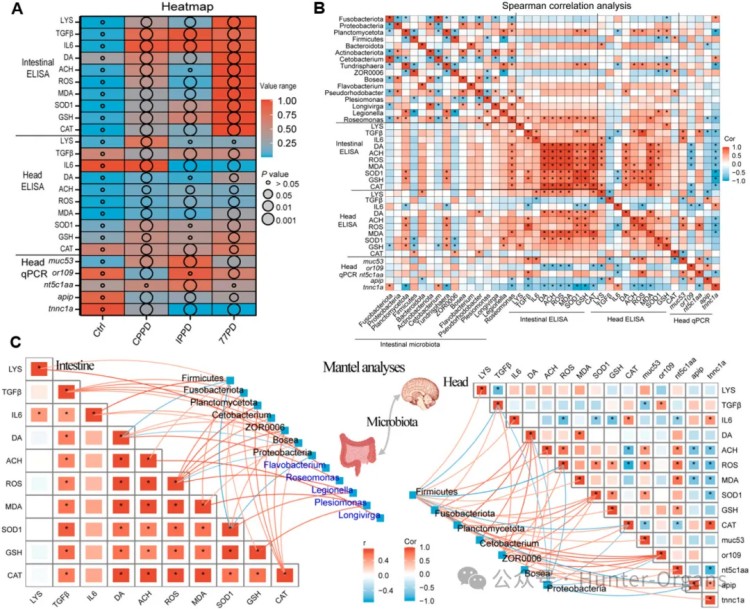
图7
6. 抗生素MTZ缓解PPDs诱导的肠-脑轴功能障碍
随后,研究人员探究了抗生素MTZ在治疗由PPDs引起的厌氧菌感染中的作用,以探索肠-脑轴的调节机制。干预实验结果显示,摄入MTZ部分缓解了PPDs诱导的斑马鱼行为改变,表现为IPPD组游泳速度降低、CPPD/IPPD组群体距离减小等。
此外,MTZ处理降低了PPDs引起的头部和肠道组织的炎症和氧化应激,表现为在PPDs头部和IPPD/77PD肠道中,LYS活性恢复到正常水平,但在CPPD肠道中则有所下降(P<0.05)。除了IPPD肠道组(P<0.05),TGFβ水平均有所下降;IL6水平均显著降低,其中,77PD的头部和CPPD的肠道下降尤为显著(P<0.05)。神经递质DA和ACH、氧化应激标志物MDA,大多降至正常水平,甚至更低。因此,抗生素甲硝唑(MTZ)干预可缓解PPDs引起的行为异常和肠-脑应激指标,进一步验证了肠-脑轴的核心作用。
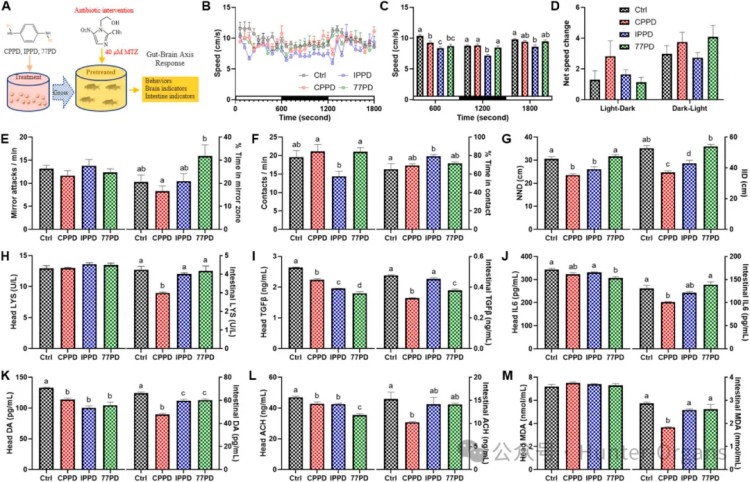
图8
近年来,环境污染问题日益严重,环境中的风险物质对生物体的健康影响备受关注。环特生物依托国际领先的斑马鱼、类器官、哺乳动物、人体临床等多维生物技术服务平台,开发了一系列评价环境中风险物质的模型,如斑马鱼胚胎急性毒性模型、甲状腺干扰效应评价模型等,为环境风险评估和人体健康保护提供科学依据。欢迎新老客户咨询!
03、编者点评
本研究首次系统评估了CPPD、IPPD、77PD这三种较少被关注的PPDs的神经毒性, 揭示了肠-脑轴功能障碍是PPDs诱导神经毒性的关键环节,证实了胚胎期斑马鱼暴露于这三种PPDs均能诱导显著的神经行为学改变和生长抑制、直接损伤脑眼轴神经细胞和肠道、诱导肠道结构破坏和功能障碍,并引起氧化应激、炎症反应、神经递质失衡及特定基因表达改变,以及肠道菌群失调等。这些发现与先前关于6PPD及其醌类代谢物的研究结果在某些方面具有一致性,为理解环境污染物的毒性机制提供了新视角。
作为健康美丽产业CRO服务开拓者与引领者、斑马鱼生物技术的全球领导者,环特生物搭建了“斑马鱼、基因编辑、类器官、哺乳动物、人体”等多维生物技术服务体系,开展健康美丽CRO服务、科研服务、智慧实验室搭建三大业务。目前,环特已建立200多种斑马鱼模型,脑类器官、胃癌、心脏类器官及各种肿瘤类器官培养平台,欢迎有需要的读者垂询!
参考文献:
Minyan Xu,Jiangfei Chen, et al. Gut-brain axis dysfunction mediates neurotoxicity of embryonic p-phenylenediamine exposure in zebrafish. J Hazard Mater.2025. DOI: 10.1016/j.jhazmat.2025.139650